

作用機序剤形血中半減期
(健康成人) コメント
ヒトの尿中に存在するプラスミノゲンアクチベーター.プラスミノゲンのpeptide結合
を開裂させて蛋白分解活性を有するプラスミンを生成する.生成したプラスミンがフィブリンを分解することによ
り血栓および塞栓を溶解する.
注射:1バイアル中6万単位,12万単位,24万単位
12万単位冠動脈
内投与:第1相6.8分,
第2相4.4時間,24万単位:第1相5.7分,第2相4.3時間
血栓溶解療法は血栓症の超急性期に行う.梗塞発現後6時間以上を経過している場合は,臨床的な改善が期待できない.
循環血液中の線溶活性を亢進させる.フィブリン親和性が低いため,出血の副作用が問題となる.全身投与よりも血栓近傍への局所投与が有用である.投与法は末梢静脈投与と冠動脈内投与がある.
フィブリン親和性が高く,血栓に特異的に吸着し血栓上でプラスミノゲンをプラスミンに転化させ,これがフィブリ
ンを分解し,血栓を溶解する.
注射:1バイアル
中600万I.U.
1,200万I.U.
2,400万I.U.
T1/2α:6.3士2分
T1/2β:84.2士48分
フィブリン親和性が高く,ウロキナーゼに比べて出血の副作用が少ない.
投与は発症後できるだけ早期に行う.
脳出血による死亡例が認められているため,適応患者の選択を慎重に行い,出血性有害事象の発現に十分注意して経過観察を行う.
胸部大動脈解離あるいは胸部大動脈瘤を合併している可能性がある患者では適応を十分に検討する.
10mL(改変型t-PAt-PAの分子構造を改変することにより,半減期が長く,総投与量を減らした急速単回投
与が可能となり,出血傾向の危険性がさらに低下
注射:1バイアル
中40万I.U.
80万I.U.
160万I.U.
T1/2α:23.66士5.2分,T1/2β:7.82士0.6時間
発症後できるだけ早期に投与する.本剤により脳出血が起こることがあるため,適用患者の選択を慎重に行うとともに,投与後の患者の出血の有無を十分に確認する.
(健康成人) コメント
ヒトの尿中に存在するプラスミノゲンアクチベーター.プラスミノゲンのpeptide結合
を開裂させて蛋白分解活性を有するプラスミンを生成する.生成したプラスミンがフィブリンを分解することによ
り血栓および塞栓を溶解する.
注射:1バイアル中6万単位,12万単位,24万単位
12万単位冠動脈
内投与:第1相6.8分,
第2相4.4時間,24万単位:第1相5.7分,第2相4.3時間
血栓溶解療法は血栓症の超急性期に行う.梗塞発現後6時間以上を経過している場合は,臨床的な改善が期待できない.
循環血液中の線溶活性を亢進させる.フィブリン親和性が低いため,出血の副作用が問題となる.全身投与よりも血栓近傍への局所投与が有用である.投与法は末梢静脈投与と冠動脈内投与がある.
フィブリン親和性が高く,血栓に特異的に吸着し血栓上でプラスミノゲンをプラスミンに転化させ,これがフィブリ
ンを分解し,血栓を溶解する.
注射:1バイアル
中600万I.U.
1,200万I.U.
2,400万I.U.
T1/2α:6.3士2分
T1/2β:84.2士48分
フィブリン親和性が高く,ウロキナーゼに比べて出血の副作用が少ない.
投与は発症後できるだけ早期に行う.
脳出血による死亡例が認められているため,適応患者の選択を慎重に行い,出血性有害事象の発現に十分注意して経過観察を行う.
胸部大動脈解離あるいは胸部大動脈瘤を合併している可能性がある患者では適応を十分に検討する.
10mL(改変型t-PAt-PAの分子構造を改変することにより,半減期が長く,総投与量を減らした急速単回投
与が可能となり,出血傾向の危険性がさらに低下
注射:1バイアル
中40万I.U.
80万I.U.
160万I.U.
T1/2α:23.66士5.2分,T1/2β:7.82士0.6時間
発症後できるだけ早期に投与する.本剤により脳出血が起こることがあるため,適用患者の選択を慎重に行うとともに,投与後の患者の出血の有無を十分に確認する.
一般名(商品名) 心疾患に対する抗血
栓薬としての適応禁忌主な副作用投与経路・用量・用法ウロキナーゼ(ウロキナーゼ)
12万・24万単位: 急性心筋梗塞における冠動脈血栓の溶解(発症後6時間以内)
12万・24万単位:
出血している患者,2カ月以内に頭蓋内あるいは脊髄の手術又は損傷を受けた患者,頭蓋内腫瘍,
動静脈奇形,動脈瘤のある患者,出血性素因のある患者,重篤な高血圧症患者
12・24万単位: 脳出血,消化管出血,心破裂,ショック,不整脈
川崎病では10,000単位/kgを30~60分間かけて静注
(成人一日最大投与量は96万単位)
成人
12万単位:生食またはブドウ糖注射液を用いて6000単位/mL に溶解し,48~96万単位を2.4万単位/4mL/
分で冠動脈内に注入.
24万単位:96万単位を生食またはブドウ糖注射液50~200mL に溶解し,約30分間で静注.
アルテプラーゼ(遺伝子組換えt-PA製剤)
(アクチバシン・グルトパ)
急性心筋梗塞における冠動脈血栓の溶解(発症後6時間以内)
出血している患者,出血するおそれの高い患者,重篤な高血圧症の患者,
重篤な肝障害のある患者,急性膵炎の患者,本剤の成分に対して過敏症の既往歴のある患者
脳出血,消化管出血などの重篤な出血,出血性脳梗塞,ショック,アナフィラキシー様症状,心破裂,
心タンポナーデ,血管浮腫,重篤な不整脈
29 万-43.5 万I.U./kg(0.5 ~ 0.75mg/kg) を静注. 投与量上限は3,480万I.U.(60mg)まで.
総量の10%を1~2分間で急速投与し,その後残りを1時間で点滴静注する.
(ACCP ガイドラインでは0.1~0.6mg/kg/hour for 6hours を推奨)
モンテプラーゼ(遺伝子組換え改変型t-PA製剤)
(クリアクター)
急性心筋梗塞における冠動脈血栓の溶解(発症後6時間以内)
出血している患者,2カ月以内に頭蓋内あるいは脊髄の手術又は障害を受けた患者,頭蓋内腫瘍,
動静脈奇形,動脈瘤のある患者,出血性素因のある患者,重篤な高血圧症患者
重篤な出血,心破裂,心室中隔穿孔,心タンポナーデ,心室細動,心室頻拍,ショック
80,000I.U./mLとなるように生食で溶解し,1分間あたり約10mL(800,000I.U.)の注入速度で投与.
27,500I.U./kgを静注
栓薬としての適応禁忌主な副作用投与経路・用量・用法ウロキナーゼ(ウロキナーゼ)
12万・24万単位: 急性心筋梗塞における冠動脈血栓の溶解(発症後6時間以内)
12万・24万単位:
出血している患者,2カ月以内に頭蓋内あるいは脊髄の手術又は損傷を受けた患者,頭蓋内腫瘍,
動静脈奇形,動脈瘤のある患者,出血性素因のある患者,重篤な高血圧症患者
12・24万単位: 脳出血,消化管出血,心破裂,ショック,不整脈
川崎病では10,000単位/kgを30~60分間かけて静注
(成人一日最大投与量は96万単位)
成人
12万単位:生食またはブドウ糖注射液を用いて6000単位/mL に溶解し,48~96万単位を2.4万単位/4mL/
分で冠動脈内に注入.
24万単位:96万単位を生食またはブドウ糖注射液50~200mL に溶解し,約30分間で静注.
アルテプラーゼ(遺伝子組換えt-PA製剤)
(アクチバシン・グルトパ)
急性心筋梗塞における冠動脈血栓の溶解(発症後6時間以内)
出血している患者,出血するおそれの高い患者,重篤な高血圧症の患者,
重篤な肝障害のある患者,急性膵炎の患者,本剤の成分に対して過敏症の既往歴のある患者
脳出血,消化管出血などの重篤な出血,出血性脳梗塞,ショック,アナフィラキシー様症状,心破裂,
心タンポナーデ,血管浮腫,重篤な不整脈
29 万-43.5 万I.U./kg(0.5 ~ 0.75mg/kg) を静注. 投与量上限は3,480万I.U.(60mg)まで.
総量の10%を1~2分間で急速投与し,その後残りを1時間で点滴静注する.
(ACCP ガイドラインでは0.1~0.6mg/kg/hour for 6hours を推奨)
モンテプラーゼ(遺伝子組換え改変型t-PA製剤)
(クリアクター)
急性心筋梗塞における冠動脈血栓の溶解(発症後6時間以内)
出血している患者,2カ月以内に頭蓋内あるいは脊髄の手術又は障害を受けた患者,頭蓋内腫瘍,
動静脈奇形,動脈瘤のある患者,出血性素因のある患者,重篤な高血圧症患者
重篤な出血,心破裂,心室中隔穿孔,心タンポナーデ,心室細動,心室頻拍,ショック
80,000I.U./mLとなるように生食で溶解し,1分間あたり約10mL(800,000I.U.)の注入速度で投与.
27,500I.U./kgを静注
作用機序剤形血中半減期
(健康成人) コメント
肝臓での還元型ビタミンKの産生を阻害し,ビタミンK依存性凝固
因子( Ⅱ・VII・IX・X因子)の生成を阻害.このため,効果発現が遅い.結果としてPIVKA;
Protein induced by vitamin K antagonists が血中に出現する.
顆粒・細粒:0.2%錠
:0.5mg1mg
2mg 5mg
0.5mg:133±42時
1mg:95±27時
5mg:55±12時
先天性proteinCやproteinS欠乏症では,ワルファリン投与導入時に微小血栓による皮膚壊死を生じることがある.
多くの薬剤や食品と相互作用を示す.納豆やほうれんそうなどの緑黄色野菜やクロレラなどは,ビタミンKが多く含まれているためワルファリンの効果を減少させる.ビタミンK強化の人工乳ではワルファリン効果は減弱し,母乳栄養児では容易に効果過剰となる.吸収不良症候群や肝不全,長期の抗生剤投与でもビタミンKの欠乏が惹起されるため,ワルファリンの作用が増強される.
経口血糖降下薬,ST 合剤,H2ブロッカー,PPI,アセトアミノフェン,蛋白同化ステロイド,EM,フルコナゾール,メトロニダ
ゾールなどがワルファリン作用を増強する.肝臓でのワルファリン代謝を促進して抗凝固作用を減弱するものには,リファンピシン,カルバマゼピン,フェノバルビタールなどがある.
凝固能が異常に低下する場合の対応として,通常はワルファリンを一時中断するのみでよいが,出血症状が強い場合などはビタミンKを10~30mg静注する.効果発現には約1日を要する.
ワルファリンを長期内服している患者のほとんどは安定した用量反応を維持するが,月1回程度の定期的なモニタリングが必要である.
血液中のアンチトロンビン(AT) と特異的に結合しAT の立体構造を変化させ,トロンビンや活性化第Ⅹ因子への結合不活化速度を増加することで強力な抗凝固作用を示す
注1,000単位/mL5・10・50・100mLおよそ40分(5,000単位静注)
ヘパリンの抗凝固作用はAT が欠乏した状況下では効果が減弱するため,AT が70%以下のときはAT 製剤を併用する必要がある.
ヘパリンの影響はPT よりもAPTT に反映されるのでモニタリングは通常APTT を用いる.注射開始3時間後から,2~4時間ごとにAPTT を測定し,投与前の2倍になるように投与量を調整する.ただし,APTT 試薬の種類によりヘパリンに対する感受性が異なるため,根拠に裏付けられたものとは言い難い.ヘパリンを大量に使用する時にはAPTT では測定可能域を超えるため,ACT(Activated Coagulation Time)を用いてモニタリングする.ACTは測定手技,測定に使用した機器により得られる値に大きな差があり注意を要する.
静脈内に投与されたヘパリンの血中半減期は約40分と短く,持続的あるいは間欠的に静脈投与を行う必要がある.一方,皮下投与時には最大効果は約3時間後に出現し,約12時間持続するが,皮下投与では持続静脈投与に比較してヘパリンの生物学的利用能が著しく劣る.ヘパリン投与期間は7~10日程度が推奨されるが,その後使用される経口抗凝固薬は,作用発現までの期間を想定しヘパリン中止の5日前から併用する.ヘパリンを過剰投与した場合は,通常ヘパリンを中止するのみで十分であるが,緊急を要する場合は抗ヘパリン作用をもつ硫酸プロタミンあるいはヘパリナーゼを静注し中和する.
(健康成人) コメント
肝臓での還元型ビタミンKの産生を阻害し,ビタミンK依存性凝固
因子( Ⅱ・VII・IX・X因子)の生成を阻害.このため,効果発現が遅い.結果としてPIVKA;
Protein induced by vitamin K antagonists が血中に出現する.
顆粒・細粒:0.2%錠
:0.5mg1mg
2mg 5mg
0.5mg:133±42時
1mg:95±27時
5mg:55±12時
先天性proteinCやproteinS欠乏症では,ワルファリン投与導入時に微小血栓による皮膚壊死を生じることがある.
多くの薬剤や食品と相互作用を示す.納豆やほうれんそうなどの緑黄色野菜やクロレラなどは,ビタミンKが多く含まれているためワルファリンの効果を減少させる.ビタミンK強化の人工乳ではワルファリン効果は減弱し,母乳栄養児では容易に効果過剰となる.吸収不良症候群や肝不全,長期の抗生剤投与でもビタミンKの欠乏が惹起されるため,ワルファリンの作用が増強される.
経口血糖降下薬,ST 合剤,H2ブロッカー,PPI,アセトアミノフェン,蛋白同化ステロイド,EM,フルコナゾール,メトロニダ
ゾールなどがワルファリン作用を増強する.肝臓でのワルファリン代謝を促進して抗凝固作用を減弱するものには,リファンピシン,カルバマゼピン,フェノバルビタールなどがある.
凝固能が異常に低下する場合の対応として,通常はワルファリンを一時中断するのみでよいが,出血症状が強い場合などはビタミンKを10~30mg静注する.効果発現には約1日を要する.
ワルファリンを長期内服している患者のほとんどは安定した用量反応を維持するが,月1回程度の定期的なモニタリングが必要である.
血液中のアンチトロンビン(AT) と特異的に結合しAT の立体構造を変化させ,トロンビンや活性化第Ⅹ因子への結合不活化速度を増加することで強力な抗凝固作用を示す
注1,000単位/mL5・10・50・100mLおよそ40分(5,000単位静注)
ヘパリンの抗凝固作用はAT が欠乏した状況下では効果が減弱するため,AT が70%以下のときはAT 製剤を併用する必要がある.
ヘパリンの影響はPT よりもAPTT に反映されるのでモニタリングは通常APTT を用いる.注射開始3時間後から,2~4時間ごとにAPTT を測定し,投与前の2倍になるように投与量を調整する.ただし,APTT 試薬の種類によりヘパリンに対する感受性が異なるため,根拠に裏付けられたものとは言い難い.ヘパリンを大量に使用する時にはAPTT では測定可能域を超えるため,ACT(Activated Coagulation Time)を用いてモニタリングする.ACTは測定手技,測定に使用した機器により得られる値に大きな差があり注意を要する.
静脈内に投与されたヘパリンの血中半減期は約40分と短く,持続的あるいは間欠的に静脈投与を行う必要がある.一方,皮下投与時には最大効果は約3時間後に出現し,約12時間持続するが,皮下投与では持続静脈投与に比較してヘパリンの生物学的利用能が著しく劣る.ヘパリン投与期間は7~10日程度が推奨されるが,その後使用される経口抗凝固薬は,作用発現までの期間を想定しヘパリン中止の5日前から併用する.ヘパリンを過剰投与した場合は,通常ヘパリンを中止するのみで十分であるが,緊急を要する場合は抗ヘパリン作用をもつ硫酸プロタミンあるいはヘパリナーゼを静注し中和する.
一般名(商品名)
心疾患に対する抗血栓薬としての適応
禁忌主な副作用投与経路・用量・用法ワルファリン
(ワーファリン)
血栓塞栓症(静脈血栓症,心筋梗塞症,肺塞栓症,脳塞栓症,緩徐に進行する脳血栓症など)
の治療および予防
出血している患者,出血する可能性のある患者,重篤な肝障害・腎障害のある患者,中枢神経系の手術又は外傷後日の浅
い患者,本剤の成分に対し過敏症の既往歴のある患者,妊婦または妊娠している可能性のある婦人,
骨粗鬆症治療用ビタミンK2製剤を投与中の患者
脳出血や消化管出血などの出血性副作用,皮膚壊死,肝機能障害,黄疸,過敏症維持投与量の目安
12か月未満:0.16mg/kg/日
1歳以上-15歳未満:0.04~0.10mg/kg/日
暫定維持量の計算式:0.04×体重(kg)+0.87
日本循環器学会のガイドラインでは0.05~0.12mg/kg/日,分1,PT-INRで1.6~2.5を目標とする.
(AHAのガイドラインは0.05~0.34mg/kg/日,PT-INRは2.0~2.5を目標とする)
初回投与量を1日1回経口投与した後,数日間かけて血液凝固能検査で目標治療域に入るように用量調節し,維持投与量を決定する.ワルファリンに対する感受性には個体差が大きく,同一個人でも変化することがあるため,
定期的に血液凝固能検査を行い,維持投与量を必要に応じて調節すること.抗凝固効果の発現を急ぐ場合には,
初回投与時ヘパリン等の併用を考慮し,治療域INRの確認後2日を経てヘパリンを中止する.成人における初回
投与量は,ワルファリンカリウムとして,通常1~5mg1日1回である.
効果発現に3~7日を要するため,投与開始5~7日目にPT-INRを測定し投与量の調節を行う.
欧米ではTTR: Tagret therapeutic INR range を2.0~3.0に設定して管理されることが多い.わが国ではTTRを欧米
より0.5程度低めに設定し,PT- INRを1.6~2.5程度にコントロールすることが多い.その理由は,確立された
エビデンスがあるわけではなく経験的なもので日本人ではその強度で効果が得られており,欧米人と同等の強度
では出血の副作用の頻度が高いと考えられたためである.
同じPT-INRを維持するのに必要なワルファリンの投与量は年齢によって異なる.
ヘパリンナトリウム
(ノボ・ヘパリン,ヘパリンナトリウム注)
血栓塞栓症(静脈血栓症,心筋梗塞症,肺塞栓症,脳塞栓症,四肢動脈血栓塞栓症,手術中・術後の血栓塞栓
症など)の治療および予防
<禁忌>
出血性血液疾患,僅少な出血でも重大な結果を来すことが予想される患者
<原則禁忌>出血している患者,出血する可能性のある患者,重篤な肝障害や腎障害のある患者,
中枢神経系の手術又は外傷後日の浅い患者,本剤の成分に対し過敏症の既往のある患者,ヘパリン起因性血小板減少症
(hepar in- induced thrombocytopenia:;HIT)の既往歴のある患者
ショック,アナフィラキシー様症状,出血,血小板減少,HIT 等に伴う血小板減少・血栓症
点滴静注:当初から維持量10~20単位/kg/時を持続投与する方法と初期に急速飽和量(50単位/kg)を10分以上かけて静注し,その後維持量を持続投与する方法がある.
成人では点滴静注:10,000~30,000単位を5%ブドウ糖注射液や生食,リンゲル液1,000mLで希釈し,最初1分間30滴前後の速度で,続いて全血凝固時間又はAPTT が投与前の2-3倍になれば1分間20滴前後の速度で,点滴静注する
間欠静注法:1回5,000~10,000単位を4~8時間ごとに静注.注射開始3時間後から,2~4時間ごとに全血
凝固時間又はAPTT を測定し,投与前の2-3倍になるようにコントロール
皮下注・筋注法: 1回5,000単位を4時間ごとに皮下注又は筋注
心疾患に対する抗血栓薬としての適応
禁忌主な副作用投与経路・用量・用法ワルファリン
(ワーファリン)
血栓塞栓症(静脈血栓症,心筋梗塞症,肺塞栓症,脳塞栓症,緩徐に進行する脳血栓症など)
の治療および予防
出血している患者,出血する可能性のある患者,重篤な肝障害・腎障害のある患者,中枢神経系の手術又は外傷後日の浅
い患者,本剤の成分に対し過敏症の既往歴のある患者,妊婦または妊娠している可能性のある婦人,
骨粗鬆症治療用ビタミンK2製剤を投与中の患者
脳出血や消化管出血などの出血性副作用,皮膚壊死,肝機能障害,黄疸,過敏症維持投与量の目安
12か月未満:0.16mg/kg/日
1歳以上-15歳未満:0.04~0.10mg/kg/日
暫定維持量の計算式:0.04×体重(kg)+0.87
日本循環器学会のガイドラインでは0.05~0.12mg/kg/日,分1,PT-INRで1.6~2.5を目標とする.
(AHAのガイドラインは0.05~0.34mg/kg/日,PT-INRは2.0~2.5を目標とする)
初回投与量を1日1回経口投与した後,数日間かけて血液凝固能検査で目標治療域に入るように用量調節し,維持投与量を決定する.ワルファリンに対する感受性には個体差が大きく,同一個人でも変化することがあるため,
定期的に血液凝固能検査を行い,維持投与量を必要に応じて調節すること.抗凝固効果の発現を急ぐ場合には,
初回投与時ヘパリン等の併用を考慮し,治療域INRの確認後2日を経てヘパリンを中止する.成人における初回
投与量は,ワルファリンカリウムとして,通常1~5mg1日1回である.
効果発現に3~7日を要するため,投与開始5~7日目にPT-INRを測定し投与量の調節を行う.
欧米ではTTR: Tagret therapeutic INR range を2.0~3.0に設定して管理されることが多い.わが国ではTTRを欧米
より0.5程度低めに設定し,PT- INRを1.6~2.5程度にコントロールすることが多い.その理由は,確立された
エビデンスがあるわけではなく経験的なもので日本人ではその強度で効果が得られており,欧米人と同等の強度
では出血の副作用の頻度が高いと考えられたためである.
同じPT-INRを維持するのに必要なワルファリンの投与量は年齢によって異なる.
ヘパリンナトリウム
(ノボ・ヘパリン,ヘパリンナトリウム注)
血栓塞栓症(静脈血栓症,心筋梗塞症,肺塞栓症,脳塞栓症,四肢動脈血栓塞栓症,手術中・術後の血栓塞栓
症など)の治療および予防
<禁忌>
出血性血液疾患,僅少な出血でも重大な結果を来すことが予想される患者
<原則禁忌>出血している患者,出血する可能性のある患者,重篤な肝障害や腎障害のある患者,
中枢神経系の手術又は外傷後日の浅い患者,本剤の成分に対し過敏症の既往のある患者,ヘパリン起因性血小板減少症
(hepar in- induced thrombocytopenia:;HIT)の既往歴のある患者
ショック,アナフィラキシー様症状,出血,血小板減少,HIT 等に伴う血小板減少・血栓症
点滴静注:当初から維持量10~20単位/kg/時を持続投与する方法と初期に急速飽和量(50単位/kg)を10分以上かけて静注し,その後維持量を持続投与する方法がある.
成人では点滴静注:10,000~30,000単位を5%ブドウ糖注射液や生食,リンゲル液1,000mLで希釈し,最初1分間30滴前後の速度で,続いて全血凝固時間又はAPTT が投与前の2-3倍になれば1分間20滴前後の速度で,点滴静注する
間欠静注法:1回5,000~10,000単位を4~8時間ごとに静注.注射開始3時間後から,2~4時間ごとに全血
凝固時間又はAPTT を測定し,投与前の2-3倍になるようにコントロール
皮下注・筋注法: 1回5,000単位を4時間ごとに皮下注又は筋注
作用機序剤形血中半減期
(健康成人) コメント
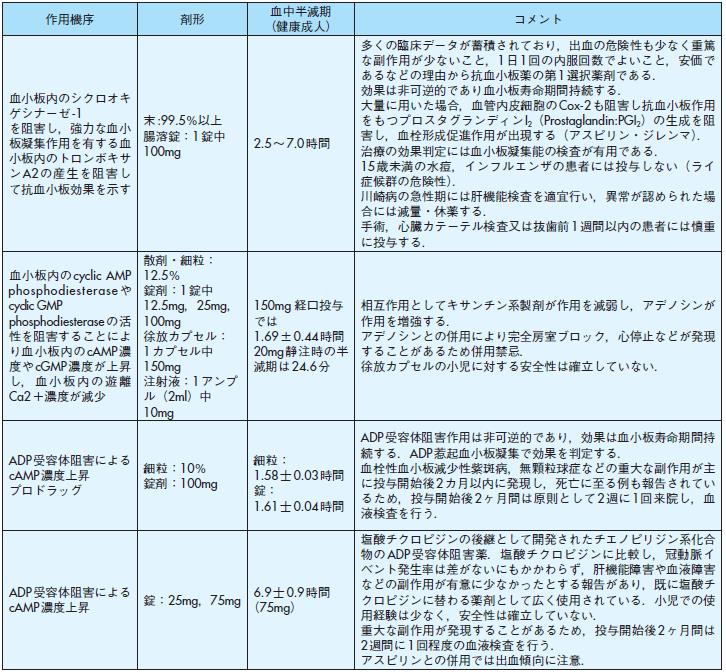
血小板内のシクロオキゲシナーゼ-1を阻害し,強力な血小板凝集作用を有する血小板内のトロンボキサ
ンA2の産生を阻害して抗血小板効果を示す
末:99.5%以上腸溶錠:1錠中
100mg 2.5~7.0時間
多くの臨床データが蓄積されており,出血の危険性も少なく重篤な副作用が少ないこと,1日1回の内服回数でよいこと,安価であるなどの理由から抗血小板薬の第1選択薬剤である.
効果は非可逆的であり血小板寿命期間持続する.
大量に用いた場合,血管内皮細胞のCox-2も阻害し抗血小板作用をもつプロスタグランディンI2(Prostaglandin:PGI2)の生成を阻害し,血栓形成促進作用が出現する(アスピリン・ジレンマ).
治療の効果判定には血小板凝集能の検査が有用である.
15歳未満の水痘,インフルエンザの患者には投与しない(ライ症候群の危険性).
川崎病の急性期には肝機能検査を適宜行い,異常が認められた場合には減量・休薬する.
手術,心臓カテーテル検査又は抜歯前1週間以内の患者には慎重に投与する.
血小板内のcyclic AMPphosphodiesterase やcyclic GMP phosphodiesteraseの活性を阻害することによ
り血小板内のcAMP 濃度やcGMP 濃度が上昇し, 血小板内の遊離Ca2+濃度が減少散剤・細粒:12.5%
錠剤:1錠中12.5mg,25mg,100mg
徐放カプセル:1カプセル中150mg
注射液:1アンプル(2ml)中10mg
150mg 経口投与では1.69±0.44時間
20mg静注時の半減期は24.6分
相互作用としてキサンチン系製剤が作用を減弱し,アデノシンが作用を増強する.
アデノシンとの併用により完全房室ブロック,心停止などが発現することがあるため併用禁忌.
徐放カプセルの小児に対する安全性は確立していない.
ADP 受容体阻害によるcAMP 濃度上昇
プロドラッグ
細粒:10%
錠剤:100mg
細粒:1.58士0.03時間
錠:1.61士0.04時間
ADP 受容体阻害作用は非可逆的であり,効果は血小板寿命期間持続する.ADP 惹起血小板凝集で効果を判定する.
血栓性血小板減少性紫斑病,無顆粒球症などの重大な副作用が主に投与開始後2カ月以内に発現し,死亡に至る例も報告されているため,投与開始後2ヶ月間は原則として2週に1回来院し,血液検査を行う.
ADP 受容体阻害によるcAMP 濃度上昇錠:25mg,75mg 6.9士0.9時間(75mg)
塩酸チクロピジンの後継として開発されたチエノピリジン系化合物のADP 受容体阻害薬.塩酸チクロピジンに比較し,冠動脈イベント発生率は差がないにもかかわらず,肝機能障害や血液障害などの副作用が有意に少なかったとする報告があり,既に塩酸チクロピジンに替わる薬剤として広く使用されている.小児での使用経験は少なく,安全性は確立していない.
重大な副作用が発現することがあるため,投与開始後2ヶ月間は2週間に1回程度の血液検査を行う.
アスピリンとの併用では出血傾向に注意.
(健康成人) コメント
血小板内のシクロオキゲシナーゼ-1を阻害し,強力な血小板凝集作用を有する血小板内のトロンボキサ
ンA2の産生を阻害して抗血小板効果を示す
末:99.5%以上腸溶錠:1錠中
100mg 2.5~7.0時間
多くの臨床データが蓄積されており,出血の危険性も少なく重篤な副作用が少ないこと,1日1回の内服回数でよいこと,安価であるなどの理由から抗血小板薬の第1選択薬剤である.
効果は非可逆的であり血小板寿命期間持続する.
大量に用いた場合,血管内皮細胞のCox-2も阻害し抗血小板作用をもつプロスタグランディンI2(Prostaglandin:PGI2)の生成を阻害し,血栓形成促進作用が出現する(アスピリン・ジレンマ).
治療の効果判定には血小板凝集能の検査が有用である.
15歳未満の水痘,インフルエンザの患者には投与しない(ライ症候群の危険性).
川崎病の急性期には肝機能検査を適宜行い,異常が認められた場合には減量・休薬する.
手術,心臓カテーテル検査又は抜歯前1週間以内の患者には慎重に投与する.
血小板内のcyclic AMPphosphodiesterase やcyclic GMP phosphodiesteraseの活性を阻害することによ
り血小板内のcAMP 濃度やcGMP 濃度が上昇し, 血小板内の遊離Ca2+濃度が減少散剤・細粒:12.5%
錠剤:1錠中12.5mg,25mg,100mg
徐放カプセル:1カプセル中150mg
注射液:1アンプル(2ml)中10mg
150mg 経口投与では1.69±0.44時間
20mg静注時の半減期は24.6分
相互作用としてキサンチン系製剤が作用を減弱し,アデノシンが作用を増強する.
アデノシンとの併用により完全房室ブロック,心停止などが発現することがあるため併用禁忌.
徐放カプセルの小児に対する安全性は確立していない.
ADP 受容体阻害によるcAMP 濃度上昇
プロドラッグ
細粒:10%
錠剤:100mg
細粒:1.58士0.03時間
錠:1.61士0.04時間
ADP 受容体阻害作用は非可逆的であり,効果は血小板寿命期間持続する.ADP 惹起血小板凝集で効果を判定する.
血栓性血小板減少性紫斑病,無顆粒球症などの重大な副作用が主に投与開始後2カ月以内に発現し,死亡に至る例も報告されているため,投与開始後2ヶ月間は原則として2週に1回来院し,血液検査を行う.
ADP 受容体阻害によるcAMP 濃度上昇錠:25mg,75mg 6.9士0.9時間(75mg)
塩酸チクロピジンの後継として開発されたチエノピリジン系化合物のADP 受容体阻害薬.塩酸チクロピジンに比較し,冠動脈イベント発生率は差がないにもかかわらず,肝機能障害や血液障害などの副作用が有意に少なかったとする報告があり,既に塩酸チクロピジンに替わる薬剤として広く使用されている.小児での使用経験は少なく,安全性は確立していない.
重大な副作用が発現することがあるため,投与開始後2ヶ月間は2週間に1回程度の血液検査を行う.
アスピリンとの併用では出血傾向に注意.
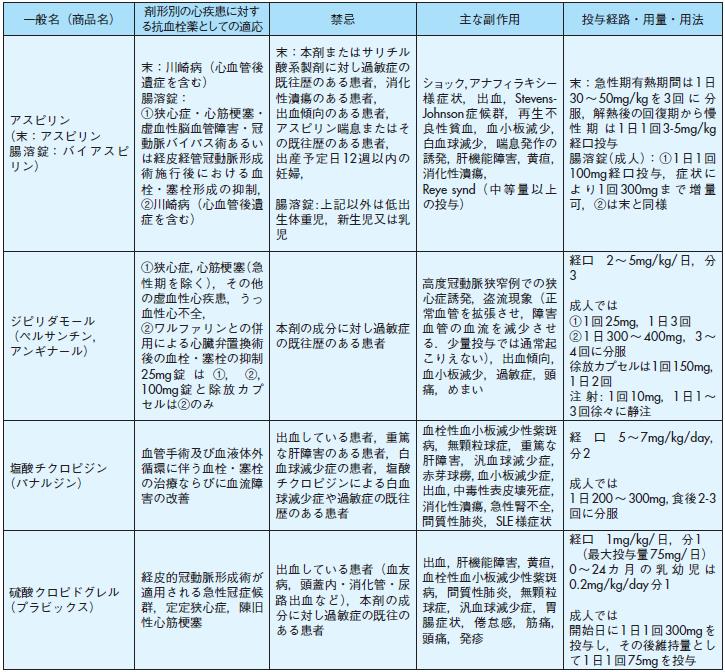
一般名(商品名) 剤形別の心疾患に対する抗血栓薬としての適応禁忌主な副作用投与経路・用量・用法アスピリン
(末:アスピリン腸溶錠:バイアスピリン)
末:川崎病(心血管後遺症を含む)
腸溶錠:
①狭心症・心筋梗塞・虚血性脳血管障害・冠動脈バイパス術あるいは経皮経管冠動脈形成術施行後における血
栓・塞栓形成の抑制,
②川崎病(心血管後遺症を含む)
末:本剤またはサリチル酸系製剤に対し過敏症の既往歴のある患者,消化性潰瘍のある患者,出血傾向のある患者,
アスピリン喘息またはその既往歴のある患者,出産予定日12週以内の妊婦,
腸溶錠:上記以外は低出生体重児,新生児又は乳児
ショック,アナフィラキシー様症状, 出血,Stevens-Johnson症候群,再生不良性貧血,血小板減少,
白血球減少,喘息発作の誘発,肝機能障害,黄疸,消化性潰瘍,
Reye synd( 中等量以上の投与)
末:急性期有熱期間は1日30~50mg/kgを3回に分服,解熱後の回復期から慢性期は1日1回3-5mg/kg経口投与
腸溶錠(成人):①1日1回100mg経口投与, 症状により1回300mgまで増量可,②は末と同様
ジピリダモール( ペルサンチン,アンギナール)
①狭心症,心筋梗塞(急性期を除く),その他の虚血性心疾患,うっ血性心不全,
②ワルファリンとの併用による心臓弁置換術後の血栓・塞栓の抑制
25mg錠は①, ②,100mg錠と除放カプセルは②のみ
本剤の成分に対し過敏症の既往歴のある患者高度冠動脈狭窄例での狭心症誘発,盗流現象(正常血管を拡張させ,障害
血管の血流を減少させる.少量投与では通常起こりえない),出血傾向,血小板減少,過敏症,頭痛,めまい
経口 2~5mg/kg/日,分3
成人では
①1回25mg,1日3回
② 1 日300 ~ 400mg,3 ~4回に分服
徐放カプセルは1回150mg,1日2回
注射: 1回10mg,1日1~3回徐々に静注
塩酸チクロピジン(パナルジン)
血管手術及び血液体外循環に伴う血栓・塞栓の治療ならびに血流障害の改善
出血している患者,重篤な肝障害のある患者,白血球減少症の患者,塩酸チクロピジンによる白血球減少症や過敏症の既往
歴のある患者
血栓性血小板減少性紫斑病,無顆粒球症,重篤な肝障害,汎血球減少症,赤芽球癆,血小板減少症,
出血,中毒性表皮壊死症,消化性潰瘍,急性腎不全,間質性肺炎,SLE様症状
経口 5~7mg/kg/day,分2
成人では
1日200~300mg,食後2-3回に分服
硫酸クロピドグレル(プラビックス)
経皮的冠動脈形成術が適用される急性冠症候群,定定狭心症,陳旧性心筋梗塞
出血している患者(血友病,頭蓋内・消化管・尿路出血など),本剤の成分に対し過敏症の既往のある患者
出血,肝機能障害,黄疸,血栓性血小板減少性紫斑病,間質性肺炎,無顆粒球症,汎血球減少症,胃腸症状,倦怠感,筋痛,
頭痛,発疹
経口 1mg/kg/日,分1
(最大投与量75mg/日)
0~24カ月の乳幼児は0.2mg/kg/day 分1
成人では
開始日に1日1回300mgを投与し,その後維持量として1日1回75mgを投与
(末:アスピリン腸溶錠:バイアスピリン)
末:川崎病(心血管後遺症を含む)
腸溶錠:
①狭心症・心筋梗塞・虚血性脳血管障害・冠動脈バイパス術あるいは経皮経管冠動脈形成術施行後における血
栓・塞栓形成の抑制,
②川崎病(心血管後遺症を含む)
末:本剤またはサリチル酸系製剤に対し過敏症の既往歴のある患者,消化性潰瘍のある患者,出血傾向のある患者,
アスピリン喘息またはその既往歴のある患者,出産予定日12週以内の妊婦,
腸溶錠:上記以外は低出生体重児,新生児又は乳児
ショック,アナフィラキシー様症状, 出血,Stevens-Johnson症候群,再生不良性貧血,血小板減少,
白血球減少,喘息発作の誘発,肝機能障害,黄疸,消化性潰瘍,
Reye synd( 中等量以上の投与)
末:急性期有熱期間は1日30~50mg/kgを3回に分服,解熱後の回復期から慢性期は1日1回3-5mg/kg経口投与
腸溶錠(成人):①1日1回100mg経口投与, 症状により1回300mgまで増量可,②は末と同様
ジピリダモール( ペルサンチン,アンギナール)
①狭心症,心筋梗塞(急性期を除く),その他の虚血性心疾患,うっ血性心不全,
②ワルファリンとの併用による心臓弁置換術後の血栓・塞栓の抑制
25mg錠は①, ②,100mg錠と除放カプセルは②のみ
本剤の成分に対し過敏症の既往歴のある患者高度冠動脈狭窄例での狭心症誘発,盗流現象(正常血管を拡張させ,障害
血管の血流を減少させる.少量投与では通常起こりえない),出血傾向,血小板減少,過敏症,頭痛,めまい
経口 2~5mg/kg/日,分3
成人では
①1回25mg,1日3回
② 1 日300 ~ 400mg,3 ~4回に分服
徐放カプセルは1回150mg,1日2回
注射: 1回10mg,1日1~3回徐々に静注
塩酸チクロピジン(パナルジン)
血管手術及び血液体外循環に伴う血栓・塞栓の治療ならびに血流障害の改善
出血している患者,重篤な肝障害のある患者,白血球減少症の患者,塩酸チクロピジンによる白血球減少症や過敏症の既往
歴のある患者
血栓性血小板減少性紫斑病,無顆粒球症,重篤な肝障害,汎血球減少症,赤芽球癆,血小板減少症,
出血,中毒性表皮壊死症,消化性潰瘍,急性腎不全,間質性肺炎,SLE様症状
経口 5~7mg/kg/day,分2
成人では
1日200~300mg,食後2-3回に分服
硫酸クロピドグレル(プラビックス)
経皮的冠動脈形成術が適用される急性冠症候群,定定狭心症,陳旧性心筋梗塞
出血している患者(血友病,頭蓋内・消化管・尿路出血など),本剤の成分に対し過敏症の既往のある患者
出血,肝機能障害,黄疸,血栓性血小板減少性紫斑病,間質性肺炎,無顆粒球症,汎血球減少症,胃腸症状,倦怠感,筋痛,
頭痛,発疹
経口 1mg/kg/日,分1
(最大投与量75mg/日)
0~24カ月の乳幼児は0.2mg/kg/day 分1
成人では
開始日に1日1回300mgを投与し,その後維持量として1日1回75mgを投与
1 序文
小児を対象に抗凝固・抗血小板療法を行う場合は,小児の止血生理の特異性を理解し,成長発達の過程にあることや新生児から思春期まで体格や体重に幅があることを考慮する.小児の循環器疾患を対象とした抗凝固・抗血小板療法に対するエビデンスは皆無に近いため,限られた情報と経験に基づき個々の施設で独自の方
法が選択されているのが現状であり,ガイドライン作成においてランク付けされたエビデンスを添付することは極めて困難な状況にある.本ガイドラインの作成に際しては日本循環器学会が策定している循環器疾患における抗凝固・抗血小板療法に関するガイドライン(2009年改訂版)244)の小児領域の分野(2003年に施行されたアンケート調査によるデータベースをエビデンス情報の一つとしている),川崎病心臓血管後遺症の診断と治療に関するガイドライン(2008年改訂版)245),心房細動治療(薬物)ガイドライン(2008年改訂版)246)をもとに,American College of Chest Physicians(ACCP)の新生児と小児における抗血栓療法のガイドライン(2008年改訂版)247)を参考にした.またこれまでに行われた前方視的な無作為化比較試験でエビデンスとなる論文を検索し,小児循環器疾患を対象とした抗凝固・抗血小板療法の適応指針を作成した.
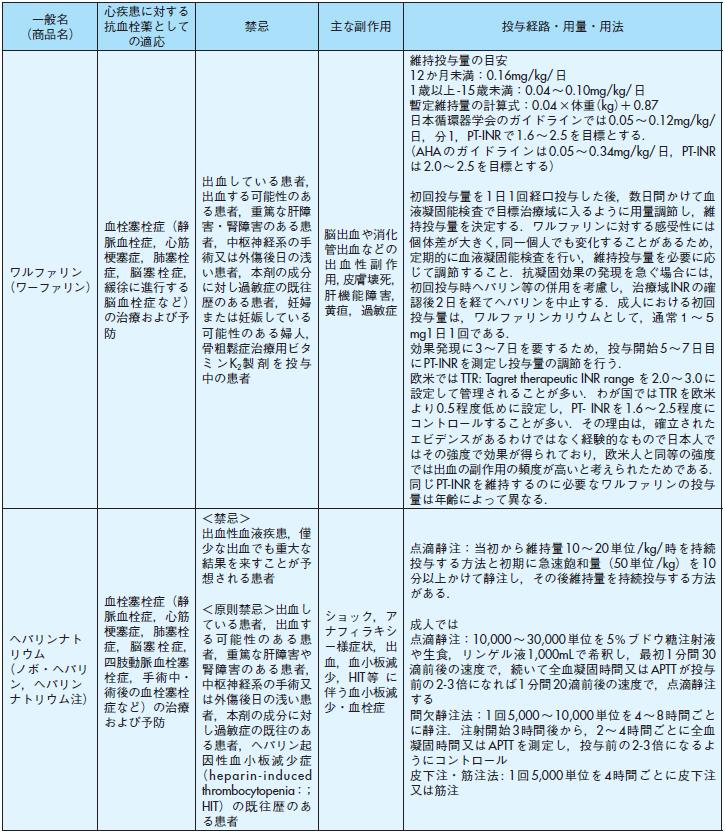
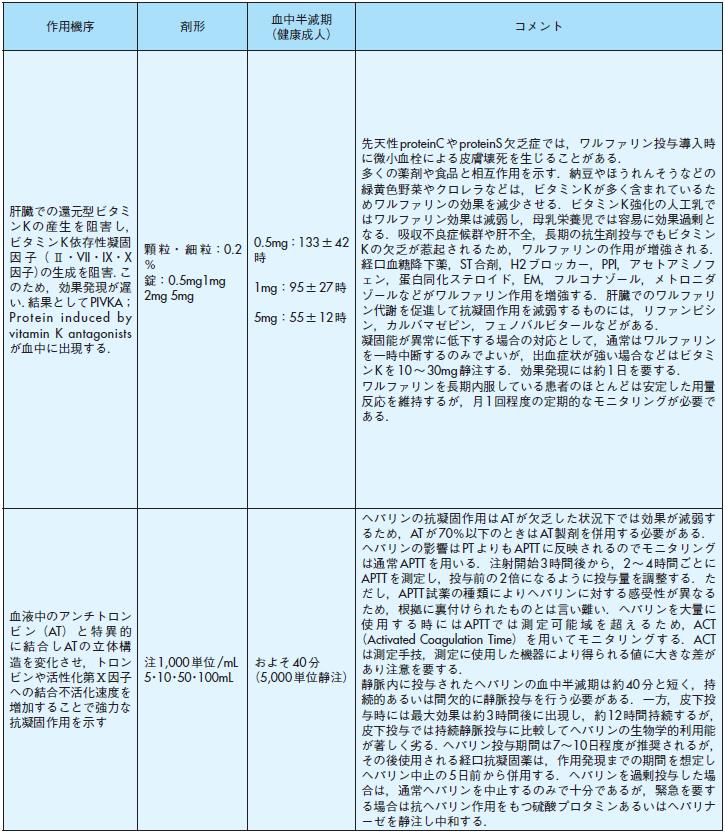
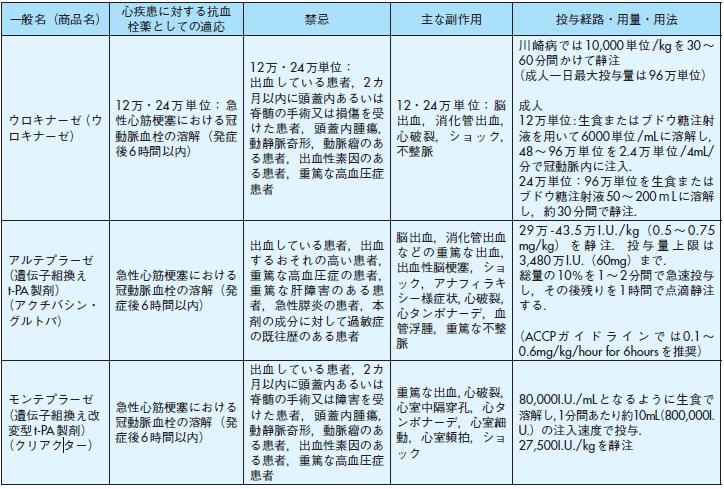
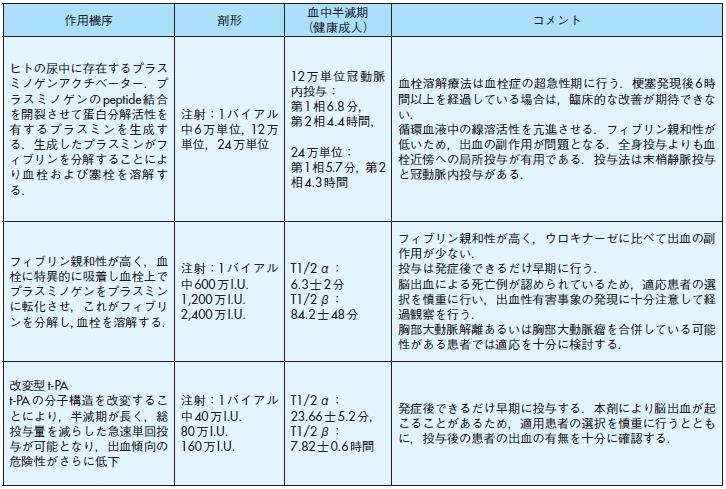
急性心筋梗塞やアテローム血栓性血栓などの動脈血栓の治療の主体は抗血小板薬であり,深部静脈血栓症や心房細動時の左房内血栓などの静脈血栓の治療の主体は抗凝固薬が主体となる.小児に抗血栓療法を行う場合,定期的かつ確実な内服が困難であること,頻回の薬効モニタリングが困難であることなど小児特有の問題が生じる.近年,経口抗トロンビン阻害薬や合成Xa 阻害薬などが次々と開発された.これらは薬効のモニタリングの必要性がなく一定の抗凝固効果が得られる利点があり,今後循環器疾患にも適応が拡大することが期待されている.現在わが国で保険適応による使用が可能な抗血栓薬(抗血小板薬,抗凝固薬,血栓溶解薬)を表12~14に示す.
抗血栓療法を行う場合には,出血性合併症の危険性を常に考慮する.個々の症例に関して抗血栓療法を行うか否かは,本ガイドラインの推奨の有無にかかわらず,十分なインフォームドコンセントのもとに個別に決定されるべきであり,ガイドラインの推奨を一律に全ての症例に適応すべきでない.近い将来,我が国でも小児を対象
としたレベルの高いエビデンスが数多く創出され,エビデンスと経験の蓄積に基づいたガイドラインの改訂がなされることを期待する.
法が選択されているのが現状であり,ガイドライン作成においてランク付けされたエビデンスを添付することは極めて困難な状況にある.本ガイドラインの作成に際しては日本循環器学会が策定している循環器疾患における抗凝固・抗血小板療法に関するガイドライン(2009年改訂版)244)の小児領域の分野(2003年に施行されたアンケート調査によるデータベースをエビデンス情報の一つとしている),川崎病心臓血管後遺症の診断と治療に関するガイドライン(2008年改訂版)245),心房細動治療(薬物)ガイドライン(2008年改訂版)246)をもとに,American College of Chest Physicians(ACCP)の新生児と小児における抗血栓療法のガイドライン(2008年改訂版)247)を参考にした.またこれまでに行われた前方視的な無作為化比較試験でエビデンスとなる論文を検索し,小児循環器疾患を対象とした抗凝固・抗血小板療法の適応指針を作成した.
急性心筋梗塞やアテローム血栓性血栓などの動脈血栓の治療の主体は抗血小板薬であり,深部静脈血栓症や心房細動時の左房内血栓などの静脈血栓の治療の主体は抗凝固薬が主体となる.小児に抗血栓療法を行う場合,定期的かつ確実な内服が困難であること,頻回の薬効モニタリングが困難であることなど小児特有の問題が生じる.近年,経口抗トロンビン阻害薬や合成Xa 阻害薬などが次々と開発された.これらは薬効のモニタリングの必要性がなく一定の抗凝固効果が得られる利点があり,今後循環器疾患にも適応が拡大することが期待されている.現在わが国で保険適応による使用が可能な抗血栓薬(抗血小板薬,抗凝固薬,血栓溶解薬)を表12~14に示す.
抗血栓療法を行う場合には,出血性合併症の危険性を常に考慮する.個々の症例に関して抗血栓療法を行うか否かは,本ガイドラインの推奨の有無にかかわらず,十分なインフォームドコンセントのもとに個別に決定されるべきであり,ガイドラインの推奨を一律に全ての症例に適応すべきでない.近い将来,我が国でも小児を対象
としたレベルの高いエビデンスが数多く創出され,エビデンスと経験の蓄積に基づいたガイドラインの改訂がなされることを期待する.
表12 抗血小板薬
表13 抗凝固薬
表14 血栓溶解薬
- Home
- 各論
- Ⅱc 抗血小板薬,抗凝固薬,血栓溶解薬
- 1 序文
小児期心疾患における薬物療法ガイドライン
Guidelines for Drug Therapy in Pediatric Patients with Cardiovascular Diseases ( JCS2012)
Guidelines for Drug Therapy in Pediatric Patients with Cardiovascular Diseases ( JCS2012)